| 引用信息: |
文 章:A Sonosensitizing Nanoshuttle for Synergistic Hypoxia Relief and Immune Activation To Strengthen Sonodynamic Immunotherapy Against Triple-Negative Breast Cancer. 期 刊:ACS Nano(影响因子:16) 发表时间:2025年12月29日 作 者:Shi-Man Zhang, Bin Gui, Qianhui Liu, et al. 作者单位:武汉大学人民医院 使用产品:Mouse TNF-α ELISA kit 文章链接:https://pubs.acs.org/doi/10.1021/acsnano.5c16697 |

基于超声的肿瘤治疗效果因肿瘤缺氧和免疫抑制微环境而大受影响。为解决这一问题,本研究通过将载氧全氟碳化物(PFC)和干扰素基因刺激蛋白(STING)激动剂DMXAA共包封于PCN222-Mn金属-有机框架中,并随后进行透明质酸(HA)修饰以实现肿瘤靶向递送,构建了一种声敏纳米穿梭体(DPPM@HA)。全身给药后,DPPM@HA在肿瘤部位积聚,并被肿瘤细胞特异性内吞。超声(US)辐照促进DPPM@HA释放氧气,从而缓解缺氧和免疫抑制,同时,充足的氧供与DPPM@HA中锰-四羧基苯基卟啉(Mn-TCPP)的超声增敏作用共同促进了细胞毒性活性氧(ROS)的大量生成,加剧了超声诱导的肿瘤损伤,并引发严重的免疫原性肿瘤细胞死亡。于此同时,框架中的高价态锰被谷胱甘肽消耗并还原为Mn2+,从而促进DPPM@HA的解体,释放出所包封的DMXAA。生成的Mn2+与DMXAA协同作用,激活STING通路,增强下游免疫应答。除了DPPM@HA介导的声动力免疫疗法对单侧肿瘤的抑制作用外,其与免疫检查点阻断的协同作用进一步增强了全身抗肿瘤免疫,对远端肿瘤和转移瘤具有显著疗效。综上所述,所提出的DPPM@HA介导的声动力免疫疗法为实现高效声动力免疫治疗提供了一种有前景的策略。
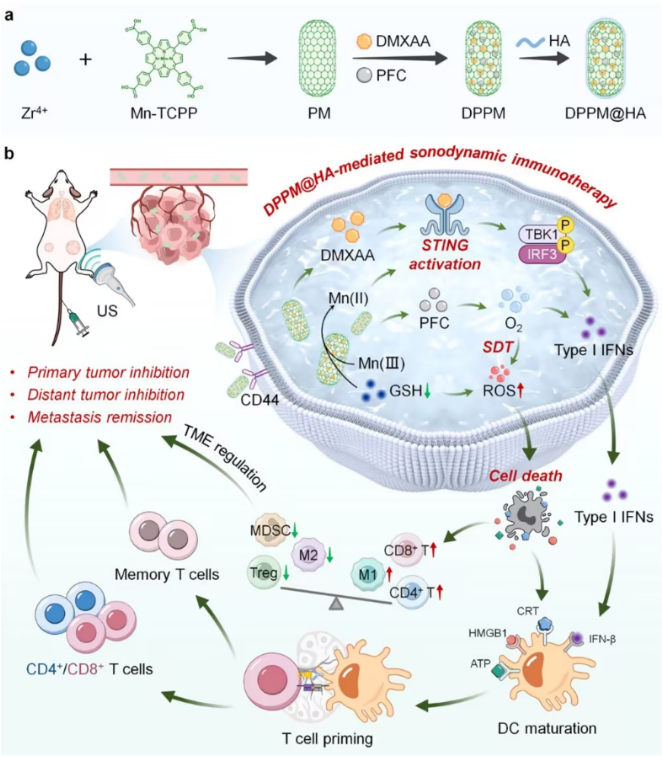
图1. DPPM@HA的合成及作用机制示意图
引用文献
Shi-Man Zhang, Bin Gui, Qianhui Liu, et al. A Sonosensitizing Nanoshuttle for Synergistic Hypoxia Relief and Immune Activation To Strengthen Sonodynamic Immunotherapy Against Triple-Negative Breast Cancer. 2026 Jan 13;20(1):1086-1102
相关产品
该项研究中,使用了欣博盛生物(NeoBioscience Technology Co, Ltd)的Mouse TNF-α、ELISA试剂盒,用于检测样本中相关因子的含量。
货号 | 产品名称 | 灵敏度 | 检测范围 |
QuantiCyto® Mouse TNF-α ELISA kit | 15.6pg/ml | 31.25-2000pg/ml |





